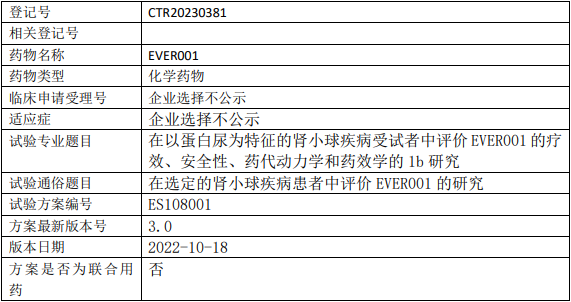
云顶新耀EVER001临床试验,评价EVER001胶囊(XNW1011)治疗以蛋白尿为特征的肾小球疾病疗效、安全性、药代动力学和药效学的Ib期临床试验
试验目的
一项在选定的以蛋白尿为特征的肾小球疾病受试者中评价EVER001的疗效、安全性、药代动力学和药效学的1b研究。
试验设计
试验分类:安全性和有效性
试验分期:I期
设计类型:单臂试验
随机化:非随机化
盲法:开放
试验范围:国内试验
受试者信息
年龄:18岁(最小年龄)至65岁(最大年龄)
性别:男+女
健康受试者:无
出入排标准
入选标准
1、年龄在18到65岁(包含两端)。
2、在过去7年内经活检确诊为原发性膜性肾病。
3、蛋白尿≥3.5g/24h;血清白蛋白>25g/L;肾小球滤过率估计值eGFR≥60mL/min/1.73m2。
4、一定时间内未接受过利妥昔单抗,之前从未接受过其他抗B细胞靶向治疗,半年内未接受过环磷酰胺治疗,3个月内未接受免疫抑制剂/免疫调节剂及静脉内免疫球蛋白。
排除标准
1、非原发性膜性肾病或存在累及肾脏的其他疾病。
2、血清白蛋白水平≤25g/l。
3、eGFR<60mL/min/1.73m2或肾功能不稳定。
4、接受过除利妥昔单抗外的B细胞靶向治疗;2年内接受过利妥昔单抗和其生物类似药(第1天前1-2年内接受利妥昔单抗或其生物类似药治疗的受试者,如果有证据表明B细胞已恢复至>90%正常值下限,则有资格参加研究。);180天内接受过环磷酰胺、苯丁酸氮芥;90天内接受过霉酚酸、他克莫司、环孢素;30天内接受过大于泼尼松30 mg/天或等效剂量的糖皮质激素。
5、实验室检查异常:筛选期间WBC<3000/mm3、淋巴细胞<1000/mm3、中性粒细胞<1500/mm3、Hb<80 g/L、血小板计数<100×10^9/L、凝血酶原时间>1.5×正常值上限(ULN)、活化部分凝血活酶时间≥1.5×ULN、天门冬氨酸氨基转移酶和丙氨酸氨基转移酶≥1.5×ULN;碱性磷酸酶和胆红素>1.5×ULN。
6、研究者判断受试者不太可能依从研究程序、限制和要求。
