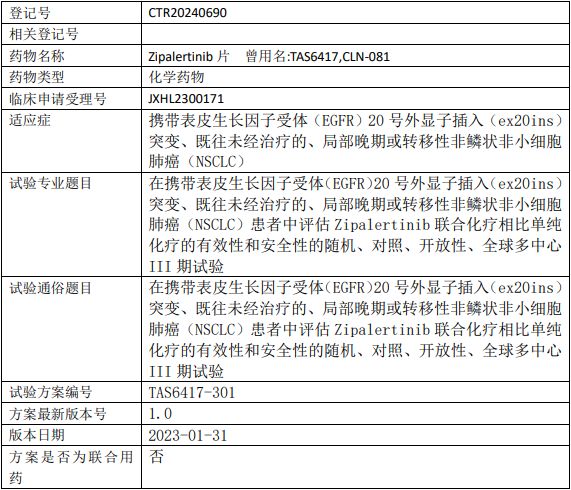
再鼎医药Zipalertinib临床试验,评估Zipalertinib(TAS6417、CLN-081、泽帕厄替尼)联合化疗相比单纯化疗治疗EGFR ex20ins突变、既往未经治疗的、局部晚期或转移性非鳞状非小细胞肺癌有效性和安全性的III期临床试验
试验目的
主要目的
比较治疗组之间的无进展生存期(PFS)。
次要目的
1、进一步比较治疗组之间的有效性;
2、评价zipalertinib与化疗联用相比单纯化疗的安全性和耐受性;
3、对于接受zipalertinib治疗的患者,评价zipalertinib联合培美曲塞和铂类药物的PK特征;
4、比较治疗组间的患者报告结局(PRO)。
探索性目的
1、探索zipalertinib与培美曲塞和铂类药物联用的有效性和安全性的暴露量-效应关系;
2、评价EGFR突变状态和zipalertinib的生物标志物。
试验设计
试验分类:安全性和有效性
试验分期:III期
设计类型:平行分组
随机化:随机化
盲法:开放
试验范围:国际多中心试验
受试者信息
年龄:18岁(最小年龄)至无上限(最大年龄)
性别:男+女
健康受试者:无
出入排标准
入选标准
1、提供书面知情同意书。
2、≥18岁(或符合国家对法定成人年龄的监管定义,以较大者为准)。
3、经病理学证实的局部晚期或转移性非鳞状NSCLC
4、既往未接受过针对任何局部晚期或转移性非鳞状NSCLC的全身治疗。对于进展期或转移性疾病,允许在研究治疗首次给药前>6个月接受过针对早期NSCLC的既往辅助/新辅助治疗。
5、有记录的EGFR突变状态,由在CLIA认证实验室或同等资质实验室进行的当地检测确定,定义如下: a.A部分:ex20ins或其他非常见的单一或复合EGFR突变: b.B部分:ex20ins EGFR突变。
6、可提交存档肿瘤组织,且最低数量足以评价EGFR突变状态以及(如可能)其他生物标志物。在与申办者讨论后,组织量不足的患者(详见实验室手册)可能符合条件;不要求重新活检。
7、既往接受过治疗的脑转移和稳定的CNS疾病(定义为神经功能稳定,在入组时接受稳定或减少的皮质类固醇剂量给药)的患者有资格参加研究。
8、根据RECIST 1.1确定至少有一处可测量病灶的患者有资格入组B部分。入组A部分的患者可在无可测量病灶的情况下入组。
9、美国东部肿瘤协作组(ECOG)体能状态评分为0或1。
10、器官功能良好,根据以下实验室检查值确定:
●中性粒细胞绝对计数(ANC):≥1500/mm3(≥1.5×109/L);
●血小板:≥100,000/mm3(≥100×109/L),研究治疗首次给药前14天内未输注血小板;
●血红蛋白:≥9.0 g/dL,研究治疗首次给药前14天内未输血; 计算的肌酐清除率(CrCl):≥50 mL/min;
●使用Cockcroft-Gault公式计算CrCl,国际标准化比值(INR)或凝血酶原时间(PT):≤1.5×正常值上限(ULN),除非患者正在接受抗凝治疗; 活化部分凝血活酶时间(aPTT)或部分凝血活酶时间(PTT):≤1.5×ULN,除非患者正在接受抗凝治疗;
●血清总胆红素:≤1.5×ULN,或直接胆红素≤ULN(对于总胆红素水平>1.5×ULN的患者),或≤3.0×ULN(对于记录有吉尔伯特综合征的患者);
●天门冬氨酸氨基转移酶(AST)和丙氨酸氨基转移酶(ALT):≤2.5×ULN或≤5×ULN(对于肝转移患者);
●碱性磷酸酶(ALP):≤3×ULN或≤5×ULN(对于肝转移患者)。
11、经研究者评估,预期寿命至少为3个月。
12、有生育能力的女性(WOCBP)在研究治疗首次给药前的血清妊娠试验结果必须为阴性;如果女性患者处于绝经后状态(12个月无月经,无其他医学原因)或永久绝育(子宫切除、双侧输卵管切除术或双侧卵巢切除术),则认为其无生育能力。
13、根据当地要求,有生育能力的男性和女性必须同意在研究期间首次给药前和研究治疗末次给药后6个月或更长时间内采取有效的避孕措施。
排除标准
1、目前正在接受临床试验中的研究性药物,或参与被认为与本研究在科学或医学上不相容的任何其他类型的医学研究。
2、在规定的特定时间范围内接受过以下任何既往治疗:
a.在任何时间接受zipalertinib(TAS6417/CLN-081);
b.胸部放疗≤28天,非胸部疾病姑息性放疗≤14天,或研究治疗首次给药前单独病灶姑息性放疗≤7天;
c.研究治疗首次给药前≤28天内进行过大手术(不包括血管通路置入)。
3、在新辅助或辅助治疗背景下,既往抗癌治疗后任何≥2级的毒性(2级脱发或皮肤色素沉着除外)未消退。在研究者和申办者商定后,可能允许有其他慢性但稳定的2级毒性的患者入组。
4、有间质性肺疾病、治疗相关肺炎(任何级别)既往病史,或有任何临床活动性间质性肺疾病的证据。
5、心脏功能受损或患有临床意义的心脏疾病,包括以下任何一种:
a.根据纽约心脏病协会(NYHA)心功能分级,有充血性心力衰竭(CHF)III/IV级病史(附录A);
b.需要治疗的严重心律失常类疾病;
c.使用Fridericia公式(QTcF)计算的静息校正QT间期(QTc)>470 msec。
6、无法吞咽片剂/胶囊,或患有任何可能显著影响胃肠道(GI)吸收zipalertinib的疾病或病症(如炎性肠病、吸收不良综合征或既往GI切除术)。
7、研究治疗首次给药日期前≤2年有其他原发性恶性肿瘤史,除非至少符合以下标准之一:
a.经充分治疗的皮肤基底细胞癌或鳞状细胞癌;
b.乳腺癌或宫颈原位癌;
c.既往治疗过恶性肿瘤,如果该恶性肿瘤的所有治疗均在研究治疗首次给药前至少2年完成,且当前无疾病证据;
d.并发恶性肿瘤,经确定临床稳定且无需抗肿瘤治疗。
8、已知乙型肝炎、丙型肝炎或人类免疫缺陷病毒(HIV)病史,病情不稳定或治疗无法控制。 在中国,符合以下标准的患者可以参加研究:
a.既往存在HBV感染的患者,目前:
i.存在乙型肝炎核心抗体(HBcAb)且不存在乙型肝炎表面抗原(HBsAg)(既往感染过HBV或HBV感染痊愈),
ii.HBsAg阳性,且HBV-DNA未检出(非活动性既往感染HBV);
b.接受过HCV治疗且未检测到病毒量的患者;
c.接受过HIV治疗且在随机化前至少1个月内未检测到病毒量的患者。 值得注意的是,对于处于非活动性HBV感染状态或HBV感染痊愈的患者,应考虑其HBV再激活的风险,并应在随机化之前根据当地指导文件仔细评估是否需要采取HBV预防措施(如服用恩替卡韦、替诺福韦等)。
9、入组前4周内有COVID-19感染史和/或存在与既往COVID-19感染相关的持续性、有临床意义的肺部症状。
10、活动性出血性疾病。
11、已知对zipalertinib中的成分或任何结构或类别相似的药物过敏
12、在培美曲塞治疗期间无法或不愿意接受地塞米松、叶酸和/或维生素B12。
13、妊娠期或哺乳期。
14、研究者认为患者无法或不愿意依从试验程序。
