个性化树突状细胞(DC)疫苗治疗晚期肺癌使肿瘤转移病灶缩小甚至消失
肺癌是威胁人类健康和生命的发病率和死亡率增长最快的恶性肿瘤之一。目前,手术和放化疗仍然是早期肺癌的标准治疗方法。对于晚期肿瘤患者,靶向治疗药物和免疫检查点抑制剂(ICIs)显著改善了部分患者的预后。然而,那些在一线治疗中失败的晚期肿瘤患者的治疗选择有限,预后不佳。因此,控制复发性晚期肿瘤的主要目标是延长生存期、减轻症状和提高生活质量。迫切需要新的、有效的和低毒性的治疗方法。
近年来,细胞治疗这种前沿医学技术进展迅速,在晚期肺癌的治疗上也有不错的临床数据,或为晚期肺癌等癌症带来新希望。
树突状细胞(DC)作为抗原递送的载体是癌症疫苗的主要焦点。一些研究报道,负载抗原的DC疫苗比由抗原和佐剂组成的疫苗诱导更强的免疫应答。因此,用于癌症治疗的基于新抗原的DC疫苗似乎是有希望的,并且已经被广泛研究。迄今为止,基于新抗原的DC疫苗已在黑色素瘤和其他实体瘤中显示出临床成功。
2021年1月在国际期刊上发表了一篇临床研究报告,报告中说明了使用个性化的新抗原肽脉冲自体DC疫苗治疗晚期肺癌。

《PubMed》期刊截图
此项研究于2017年11月至2019年9月由华西医院和同济大学第十人民医院为试点医疗中心,总计成功入选12名患者,入选的患者是接受过大量治疗的转移性肺癌患者。候选新抗原来源于新鲜活检组织的全外显子组测序和RNA测序以及生物信息学分析。总共有12名患者参加了这项研究,总共进行了85次疫苗治疗,中值为5剂/人(范围:3-14剂/人)。
每位患者总共选择了12-30个基于肽的新抗原。所有与治疗相关的不良事件均为1-2级,没有因毒性反应导致的给药延迟。客观有效率为25%;疾病控制率为75%;中位无进展生存期为5.5个月,中位总生存期为7.9个月。该研究为新抗原疫苗治疗提供了新的证据,也为肺癌治疗提供了新的治疗机会。
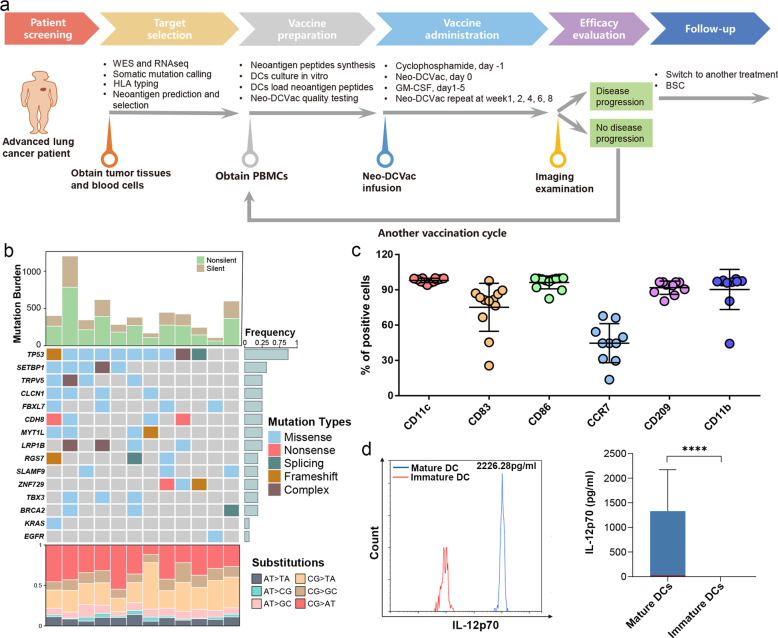
DC疫苗工作流程图、整体突变景观和DC疫苗产品分析。
DC疫苗与ICIs的协同治疗作用
在试验中共招募了4名接受过ICIs治疗的患者,这些患者要么对该治疗无反应,要么复发。在将ICIs(免疫检查点抑制剂)治疗与Neo-DCVac结合后,这些患者都实现了疾病控制(2个PRs和2个SDs),并且肿瘤大小减小了高达80%。根据临床报告,这些患者中有3人仍然健在,只有1名小细胞肺癌患者死亡,小细胞肺癌的OS比非小细胞肺癌差得多。
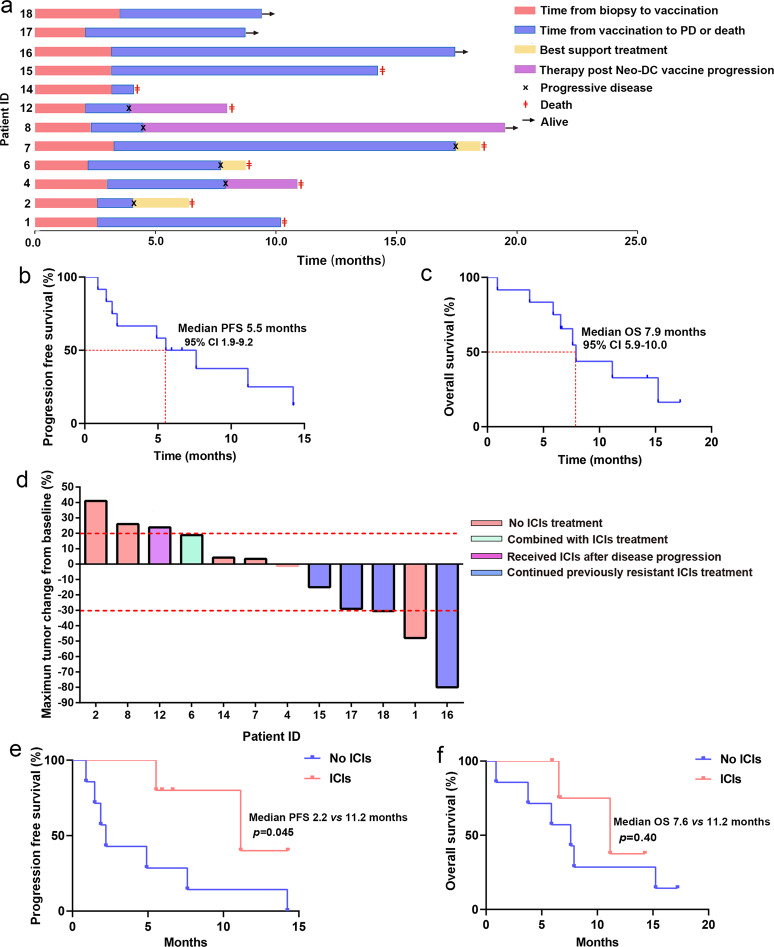
DC疫苗治疗晚期肺癌临床活性的前提分析
案例分析
患者1是一名患有转移性肺腺癌的72岁男性,在三次化疗和放疗失败后接受了个体化的Neo-DCVac治疗,该患者在三次化疗和放疗中失败,但在施用Neo-DCVac后的7.6个月中仍没有任何疾病进展的迹象。
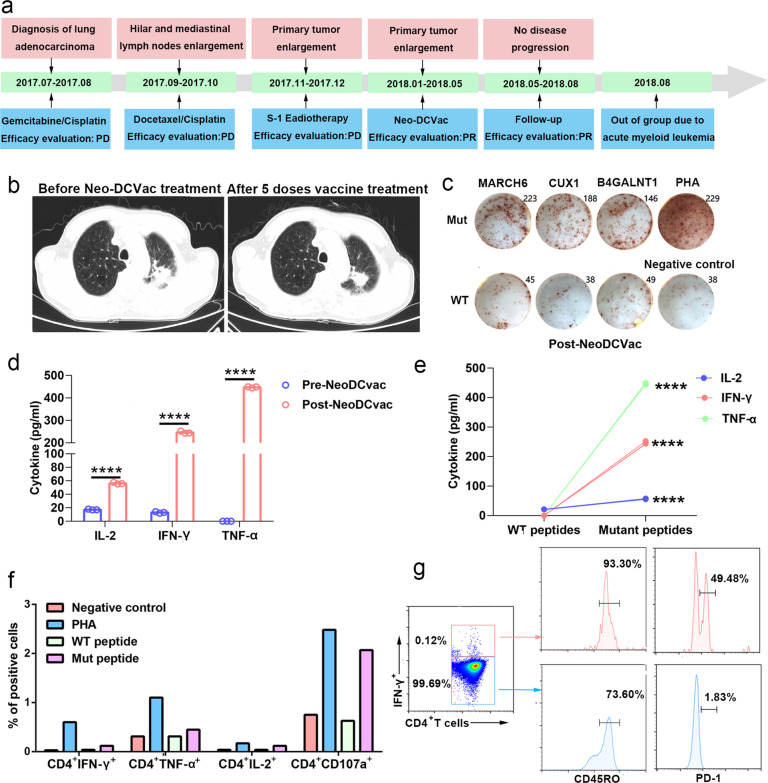
转移性肺腺癌患者1对个性化DC疫苗的免疫反应临床病程和既往治疗
患者15是患有广泛期小细胞肺癌的67岁男性,该患者在四次化疗和放疗中失败,但在使用Neo-DCVac后的11.2个月中没有任何疾病进展的迹象。
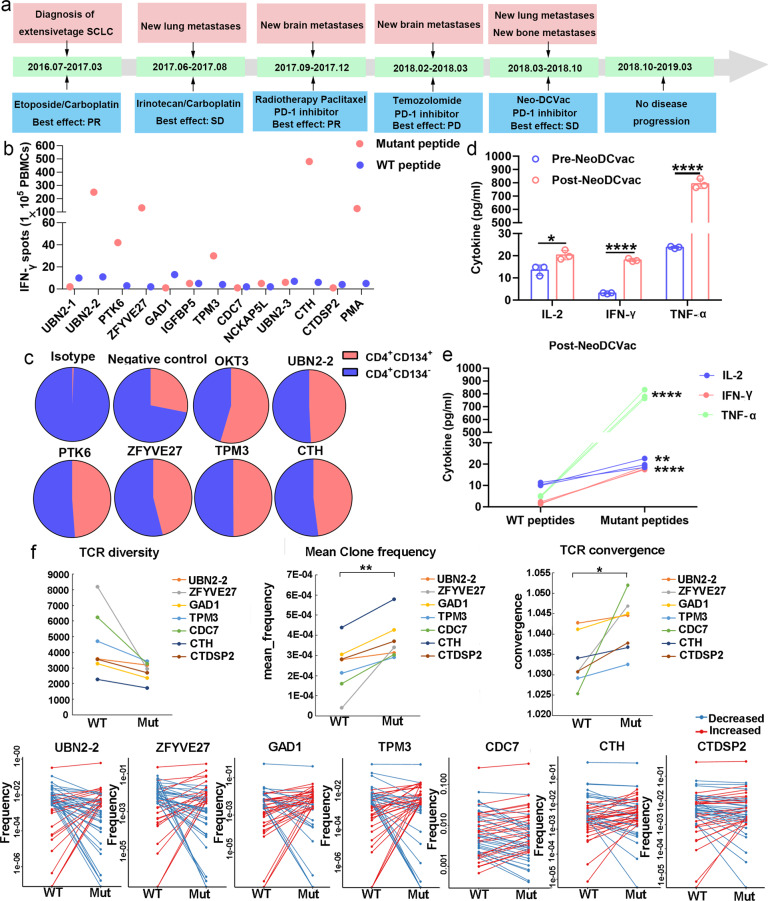
广泛期小细胞肺癌患者15对个性化DC疫苗的免疫反应、临床病程和既往治疗
患者17是患有广泛转移性肺腺癌的57岁男性。主要转移位于骨、骨盆、肾上腺和下腔静脉淋巴结。该患者在化疗、放疗和PD-1抑制剂的三线治疗中失败,并且在使用Neo-DCVac后,其肿瘤靶病变减少了29%。
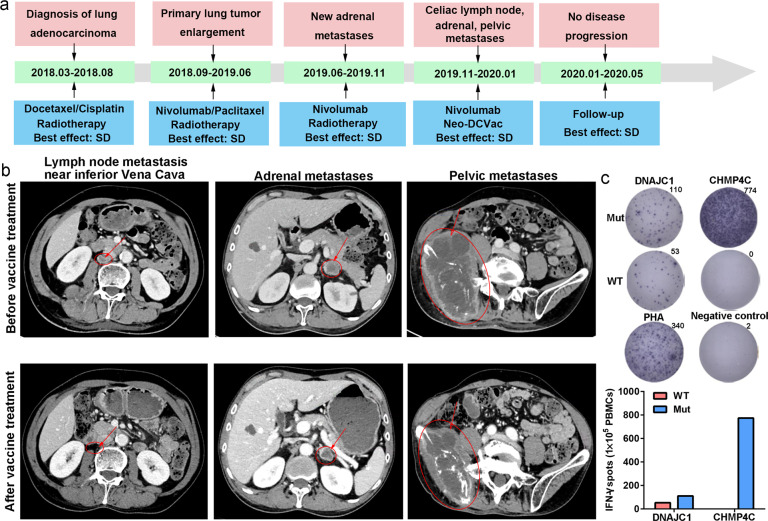
广泛期小细胞肺癌患者17对个性化DC疫苗的免疫反应、临床病程和既往治疗
对于复发性晚期肿瘤患者,探索一种既能发挥抗肿瘤作用又不增加毒副作用的治疗方法非常重要。在这项研究中,表明Neo-DCVac是安全和可耐受的,可以用于治疗晚期肺癌患者。所有的不良事件都是轻度和短暂的。更重要的是,Neo-DCVac没有增加ICI免疫治疗的严重程度,也没有诱导与ICI免疫治疗相关的其他不良事件。
这项研究表明,在接受个性化DC疫苗治疗的预处理晚期肺癌患者中,客观缓解率为25%,疾病控制率为75%。
小结
树突状细胞(DC)是人体中重要的一类免疫细胞,是已知的功能最强的抗原提呈细胞(APC)。它可以高效的提取、加工、处理并将抗原递呈给T淋巴细胞,激活机体的特异免疫,理论上可以治疗任何实体瘤。通过个性化DC疫苗的设计,特异性杀伤肿瘤。目前绝大多数都处于早期的临床试验阶段,也有像DCvax-L疫苗已经进入到Ⅲ期临床试验,显示出DC疫苗无限的治疗前景。
参考文献:Personalized neoantigen pulsed dendritic cell vaccine for advanced lung cancer。Signal Transduct Target Ther. 2021; 6: 26.
内容来源:科普细胞者
